需來院10趟吃藥5天 檢查費全免?
國家商報消息:近日,山東多家醫院,包括淄博市第一醫院,發布了《招募新型冠狀病毒肺炎患者》的相關信息。

1月4日,據大河報報道,淄博市第一醫院工作人員稱,使用的藥物是武漢市傳染病醫院研制的。一名被招募的新冠肺炎患者獲得了4000元的補貼,這需要去醫院10次,抽血3次,服藥5天。考試費是免費的。目前符合條件的患者都可以去醫院。
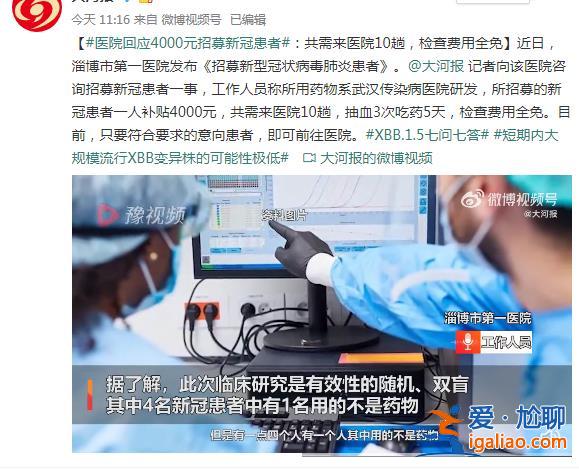
山東多家醫院招募新冠肺炎患者進行藥檢。
據山東淄博第一醫院微信號1月1日晚間消息,淄博第一醫院發布《招募新型冠狀病毒肺炎患者》稱,我院呼吸與危重癥醫學科正在開展“評價GS221治療輕癥或普通新型冠狀病毒患者安全性和有效性的隨機、雙盲、安慰劑對照臨床研究”,方案號為GS221-2022-001。這項研究現招募輕度或普通新型冠狀病毒患者,計劃在全國約20個臨床研究中心開展。在B部分中,預計將招募總共312名患者。
在這個試驗中有兩個治療組。篩選后,符合條件的受試者將按照3: 1的比例隨機接受GS221或安慰劑治療5天。每個受試者將服用溫水研究藥物,不能咀嚼。第一天口服375mg,每日一次,之后4天口服125mg<愛尬聊_百科>,每日一次,共5天。進行隨訪,直到證實核酸轉陰且所有臨床癥狀消失或研究的第14天。
淄博第一醫院表示,如果患者初步符合以下條件,請聯系他:
18年齡70周歲;
新冠肺炎被診斷為輕度和普通患者;
核酸檢測或抗原檢測呈陽性;
咳嗽、氣短或呼吸困難、發熱、發冷、疲勞、身體疼痛或肌肉疼痛、腹瀉、惡心、嘔吐、頭痛、喉嚨痛、鼻塞、流鼻涕、味覺或嗅覺喪失以及任何新冠肺炎相關癥狀;
育齡婦女入組前妊娠試驗陰性;
一個月內沒有參加其他臨床試驗。

1月2日,淄博市立醫院也發布了類似的招聘消息,消息稱:我院呼吸與危重癥醫學科正在開展“評價GS221治療輕癥或普通新型冠狀病毒患者的安全性和有效性的隨機、雙盲、安慰劑對照臨床研究”,方案號為GS221-2022-001。

據山東商報報道,近日,齊魯制藥股份有限公司也發布了其新冠肺炎口腔藥物臨床試驗的廣告,該試驗在山東大學齊魯醫院舉行。每位受試者將接受免費藥物治療,研究期為一個月。受試者無需支付研究藥物、相關檢查和治療費用,并獲得一定的試驗補償費。

據山東商報報道,淄博市第一醫院工作人員表示:“目前為每一位參與臨床研究的患者提供保險和實驗補貼。目前沒有明顯的副作用。最好的情況下,患者可以在5天內轉陰。”
據了解,目前醫院正在進行第二批試驗,之前已經進行過1:1試驗,參與臨床試驗的患者沒有受到藥物明顯副作用的影響。因此,第二批試驗將按照3:1的比例進行。消息稱,需要312人參加試驗。
藥物上市前還需要哪些條件?該工作人員表示,這批檢測完成后,還需要再檢測一次,才會上市。
一些治療藥物R&D制藥公司在新冠肺炎招募病人。
2022年12月28日晚間,遠大制藥發布公告稱,集團自主研發的抗新冠肺炎感染創新口服小分子蛋白酶抑制劑GS221于2022年9月20日獲得國家醫藥產品監督管理局頒發,并迅速開展了三項相應的臨床試驗。目前已完成的臨床試驗結果顯示,受試者的安全性和耐受性良好,未觀察到導致停藥的嚴重或不良事件。
除了遠大制藥,新冠肺炎的一些醫藥研發公司也在招聘患者,包括先聲藥業、君實生物、科興藥業
據中新經緯2022年12月28日消息,為加快治療藥物在江蘇新冠肺炎上市,江蘇美國食品藥品監督管理局副局長姜偉近日在新冠肺炎主持召開了治療藥物SIM0417研究進展專題調度會。SIM0417是由上海先聲藥業有限公司、中國科學院上海藥物研究所和中國科學院武漢病毒研究所聯合研制的3CL靶向新冠肺炎口服藥物。2022年12月16日,本項目三期1208例患者全部入組,進度居國內3CL目標藥物第一。預計最快2023年2月上市。
君實生物微信官方賬號旗下君實醫藥2022年12月16日發布的文章稱,在一項多中心、雙盲、隨機、安慰劑對照的期臨床研究中,評估JT001治療輕中度新型冠狀病毒的療效和安全性,計劃在全國招募1200名受試者。
此外,根據深圳市第三人民醫院臨床試驗中心發布的通知,眾生藥業、武漢生物制品研究所、科興藥業也于近期招募陽性患者。這三種藥物是RAY1216片劑、F61注射液和參26膠囊。
目前已有兩個新冠肺炎治療藥物獲準在中國有條件上市,分別是新冠肺炎輝瑞公司的治療藥物帕昔洛韋和河南瑞爾生物科技有限公司的阿夫定片,其中輝瑞公司的帕昔洛韋作用機制為3CL蛋白酶抑制劑。阿夫定片的作用機制是RdRp抑制劑。
